लवण: अवधारणा, गुण और उपयोग
लवण एक आयोनिक यौगिक है जो अम्ल और क्षार के उदासीनीकरण प्रक्रिया (neutralization reaction ) का परिणाम है। यह कैटायनों (सकारात्मक चार्जड आयनों) और आयनों (ऋणात्मक आयनों) के संबंधित संख्याओं के द्वारा बना है इसलिए इसका उत्पाद इलेक्ट्रिकली उदासीन (electrically neutral) अर्थार्त बिना कोई चार्ज के होता है। ये सामान्य लवण जैसे NaCl, KCl और Na2SO4; अम्ल लवण NaHCO3 और NaH2PO4 की तरह; और द्विक लवण (double salts) जैसे KAl (SO4) 2 हो सकते हैं।

दूसरे शब्दों में, लवण यौगिक होते है जो एक अम्ल परमाणु से एक धातु या एक धातु की तरह कार्य करने वाले तत्वों के द्वारा हाइड्रोजन परमाणुओं के आंशिक या पूर्ण रूप से प्रतिस्थापित होने से बनते है । उदाहरण के लिए-
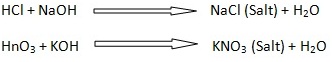
लवण के प्रकार:
सामान्य नमक (Normal Salt) : ये वह लवण होता है जो एक अम्ल परमाणु से एक धातु या एक धातु की तरह कार्य करने वाले तत्वों के द्वारा हाइड्रोजन परमाणुओं के पूर्ण रूप से प्रतिस्थापित होने से बनते है । उदाहरण: यौगिक जैसे KCl, NaCl, FeS04, Na2S04, FeCl2 आदि सामान्य लवण हैं। जाहिर है एक सामान्य लवण के परमाणु में प्रतिस्थापित योग्य H- अणु शामिल नहीं है।
क्षारीय लवण (Basic Salt): क्षारीय लवण जो अपने परमाणु में 02 – या OH- समूह रखते है उसे क्षारीय लवण कहा जाता है।उदाहरण: यौगिकें जैसे Mg (OH) Cl, [Mg(OH) 2। MgC03], [Cu (OH) 2.CuCO3) आदि क्षारीय लवण होते हैं।
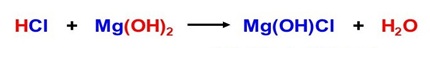
अम्लीय लवण (Acidic Salt): एक सामान्य लवण जो दृढ अम्ल और कमजोर क्षार के उदासीनीकरण द्वारा निर्मित होते है उसे अम्लीय लवण कहा जाता है। क्योंकि इसका जलीय घोल नीले लिटमस को लाल कर देता है। उदाहरण: यौगिकें जैसे FeCI3, ZnCl2, HgCl2, Fe2 (S04) 3, HgS04, NH4Cl, CuSO4 आदि अम्लीय लवण हैं।
NH4OH + HCl → NH4Cl + H2O
क्षारक लवण (Alkaline Salt) : सामान्य लवण जो कमजोर अम्ल और दृढ क्षार के उदासीनीकरण द्वारा गठित होते है उसे क्षारक लवण कहते है क्योंकि उनके जलीय घोल लाल लिटमस को नीले में बदल देता है।उदाहरण: यौगिकें जैसे Na2C03, CH3COONa, Na2C204, Na2B407.10 H20 आदि क्षारक लवण हैं।
2NaOH + H2CO3 → Na2CO3 + 2H2O
उदासीन लवण (Neutral Salt): ये मजबूत अम्ल और मजबूत क्षार के उदासीनीकरण द्वारा बनते हैं, जिसे उदासीन लवण कहते है क्योंकि उनके जलीय घोल लिटमस के लिए उदासीन होते हैं। उदाहरण: यौगिक जैसे NaCl, KCl, K2S04, NaN03, KCl03, KClO4 आदि क्षारक लवण हैं।
NaOH + HCl → NaCl + H2O
द्विक लवण (Double Salt) : एक द्विक लवण दो लवण का एक मिश्रण है जो पानी में विघटित होने पर धातु आयनों के दो प्रकार देता है। उदाहरण: यौगिक जैसे पोटाश फिटकिरी [K2S04. Al2(S04)3.24H20] , Mohr लवण [FeS04.(NH4)2S04.6H20], Ferric फिटकिरी [K2S04.Fe2 (SO4)3.24H20] आदि द्विक लवण होते हैं।
जटिल लवण (Complex Salt): ये वह लवण होते है जो एक जटिल आयन या जटिल उदासीन अणु लेते है जिसमें एक केंद्रीय धातु आयन उदासीन अणुओं या नकारात्मक आयनों की एक संख्या के द्वारा घिरा हुआ होता है।उदाहरण: यौगिक जैसे पोटेशियम फेरोसायनाइड (ferrocyanide) (K4[Fe(CN)6]), पोटेशियम argento साइनाइड (K [Ag(CN)2]) टेट्रा एमिनो cupric सल्फेट ([Cu(NH3)4]SO4) आदि जटिल लवण हैं|
लवण के उपयोग:
लवण के उपयोग तालिका के रूप में नीचे दिए गए हैं-
| लवण | उपयोग |
| सामान्य लवण (NaCl) सोडियम क्लोराइड
|
– सामान्य लवण खाना पकाने के गैस में उपयोग किया जाता है।
– यह अचार ,मांस और मछली को सुरक्षित रखने के लिए एक परिरक्षक के रूप में प्रयोग किया जाता है। – यह साबुन के निर्माण में प्रयोग किया जाता है। – यह ठंडे देशों में सर्दियों में बर्फ पिघलाने के लिए उपयोग किया जाता है। – बड़े रसायन जैसे धुलाई का सोडा, बेकिंग सोडा आदि बनाने में इस्तेमाल किया जाता है । |
| सोडियम हाइड्रॉक्साइड (NaOH) | – साबुन और डिटर्जेंट बनाने के लिए इस्तेमाल किया जाता है।
– कृत्रिम कपड़ा फाइबर (रेयान) में इस्तेमाल किया जाता है। – कागज के विनिर्माण में इस्तेमाल किया जाता है। – बाक्साइट अयस्क बनाने के लिए इस्तेमाल किया जाता है। – चिकनाई हटाने वाले धातुओं , तेल शोधन, रंजक और bleaches बनाने में इस्तेमाल किया जाता है। |
| धुलाई का सोडा (NaCO3.10 H2O) सोडियम कार्बोनेट | – ‘सफाई एजेंट’ के रूप में घरेलू प्रयोजनों के लिए कपड़ें धोने में इस्तेमाल किया जाता है।
– पानी की स्थायी कठोरता को निकालने के लिए इस्तेमाल किया जाता है। – काँच, साबुन और कागज के निर्माण में इस्तेमाल किया जाता है। – बोरेक्स (borax) जैसे सोडियम यौगिकों के निर्माण में इस्तेमाल किया जाता है। |
| बेकिंग Soda(NaHCO3) सोडियम बिकारबोनिट | – एक एंटासिड (antacid) के रूप में इस्तेमाल किया जाता है।
– बेकिंग पाउडर बनाने में इस्तेमाल किया जाता है जो कि केक, रोटी आदि बनाने में इस्तेमाल होता है। – आग बुझाने ( Fire extinguishers) में इस्तेमाल किया जाता है। |
| ब्लीचिंग पाउडर (CaOCl2) कैल्शियम हाइड्रो क्लोराइड | – वस्त्र उद्योग में कॉटन विरंजन (bleaching cotton) में, कागज और लिनन में इस्तेमाल किया जाता है।
– उद्योग मे लकड़ी के लुगदी का विरंजन(bleaching wood pulp) के लिए इस्तेमाल किया जाता है। – पीने के पानी को कीटाणुनाशक बनाने में इस्तेमाल किया जाता है। – क्लोरोफॉर्म बनाने के लिए उपयोग किया है जाता । – (CHCl3) ऊन को सिकुड़ने मे अयोग्य बनाने के रूप में इस्तेमाल किया जाता है। – कई रासायनिक उद्योगों में ऑक्सीकरण एजेंट के रूप में प्रयुक्त किया जाता है । |
| प्लास्टर ऑफ पेरिस CaS04.1/2 H2O) कैल्शियम सल्फेट hemi हाइड्रेट | – अस्पताल में टूटी हड्डीयो को जोड़ने के लिए इस्तेमाल किया जाता है।
– खिलौने, सजावट सामग्री सस्ते आभूषण, चाक आदि बनाने के लिए प्रयुक्त किया जाता है। – आग से बचाने वाले वस्तु बनाने के लिए इस्तेमाल किया जाता है। – सतह को चिकना बनाने के लिए इस्तेमाल किया जाता है। |
Science Notes के अपडेट लगातार हासिल करने के लिए हमें Facebook पर ज्वाईन करे | Click Now
Science Notes updates on Facebook joined us to continue to gain | Now click